�y�u�X�L���[�o�_�C�o�[�v�����̐g�����ׂ̗\���m���z study-four_a����̑����ł��B
���������w�@���� �H�����ŁA���M�ƒ���������܂��i*^_^*�j
�����̊�{�I�ȕ����w���q�ׂčs���܂��B
1.���� (��C���A�Ð����A��Έ��A�Q�[�W��).
2.���x�A2a.��d�A2b.���́A2c.�C���ƒW���̕s�v�c.
3.�_���g���̖@��.(�ʏ�=�����̖@��)
4.�w�����[�̖@��.
5.�ċz�K�X�̎��x�A���I�A�����蓙.
6.���̋��܁E�U���E�z���Ǝ��o�A���̌����ƌ��F.
7.�����̉�.
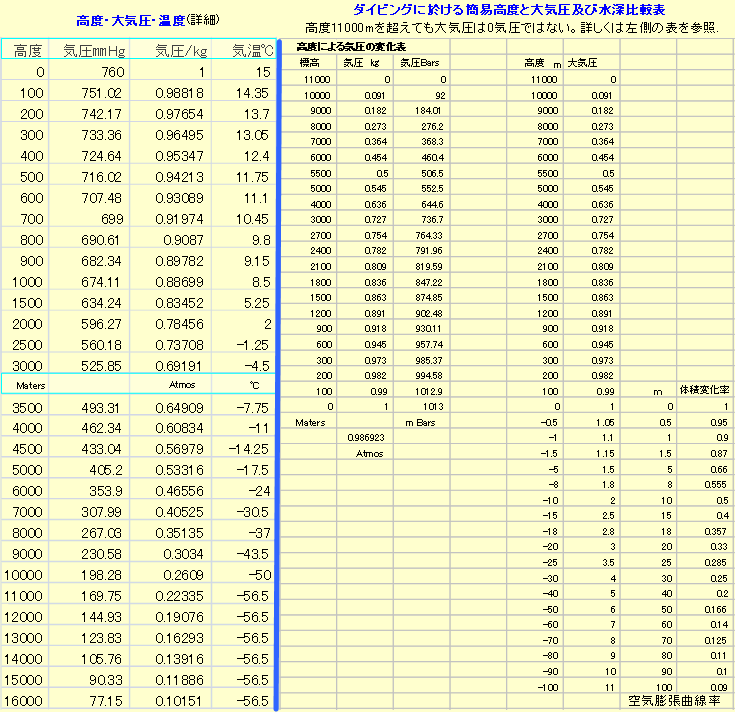
�{�C���̖@�����猩���
���x�����Ȃ�A�C�̗̂e�ς͐�Έ��͂ɔ���Ⴗ�邪�A�C�̖̂��x�͐�Έ��͂ɐ���Ⴗ��B
PV=K �@P:��Έ����@V:�e���@K:�萔
�V�������̖@�����猩���
���͂����Ȃ�A�C�̗̂e�ς͐�Ή��x�ɐ���Ⴗ��B�܂��A�e�ς����̊��҂ɉ����ẮA�C�̂̈��͂͐�Ή��x�ɐ���Ⴗ��B

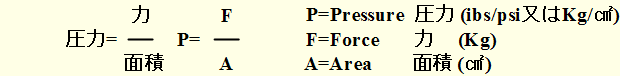
| �p�X�J���iSI�P�ʁj | �o�[�� | �H�w�C�� | �C�� | �g�� | psi | |
|---|---|---|---|---|---|---|
| 1 Pa | �� 1 N/m² | = 10-5 bar | ≈ 10.2�~10-6 at | ≈ 9.87�~10-6 atm | ≈ 7.5�~10-3 Torr | ≈ 145�~10-6 psi |
| 1 bar | = 100000 Pa | �� 106 dyn/cm² | ≈ 1.02 at | ≈ 0.987 atm | ≈ 750 Torr | ≈ 14.504 psi |
| 1 at | = 98066.5 Pa | = 0.980665 bar | �� 1 kgf/cm² | ≈ 0.968 atm | ≈ 736 Torr | ≈ 14.223 psi |
| 1 atm | = 101325 Pa | = 1.01325 bar | ≈ 1.033 at | �� p0 | = 760 Torr | ≈ 14.696 psi |
| 1 Torr | ≈ 133.322 Pa | ≈ 1.333�~10-3 bar | ≈ 1.360�~10-3 at | ≈ 1.316�~10-3 atm | �� 1 mmHg | ≈ 19.337�~10-3 psi |
| 1 psi | ≈ 6894.757 Pa | ≈ 68.948�~10-3 bar | ≈ 70.307�~10-3 at | ≈ 68.046�~10-3 atm | ≈ 51.7149 Torr | �� 1 lbf/in² |
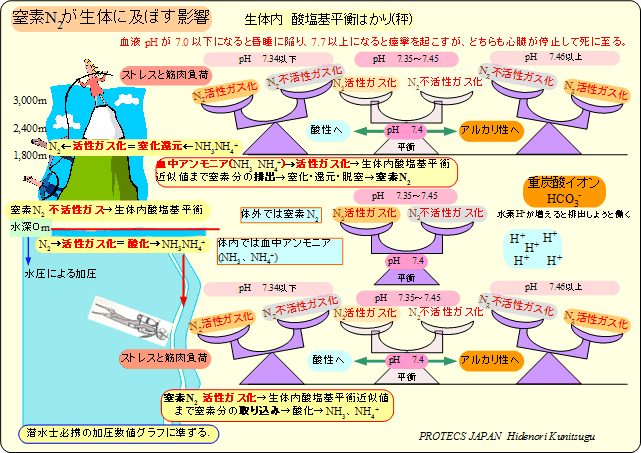
���̐}�̓_�C�o�[�̐��������ł̐����Ƌ�C���x�y�ё̐ϕω���\���Ă���B
�C��(SEA LEVEL)����Ƃ����X�L���_�C�o�[�̔x�̑̐ϕω��ŕ\���Ă���ׁA�X�L���[�o�_�C�o�[�ł͎Q�l�ɗ��߂ĉ������B
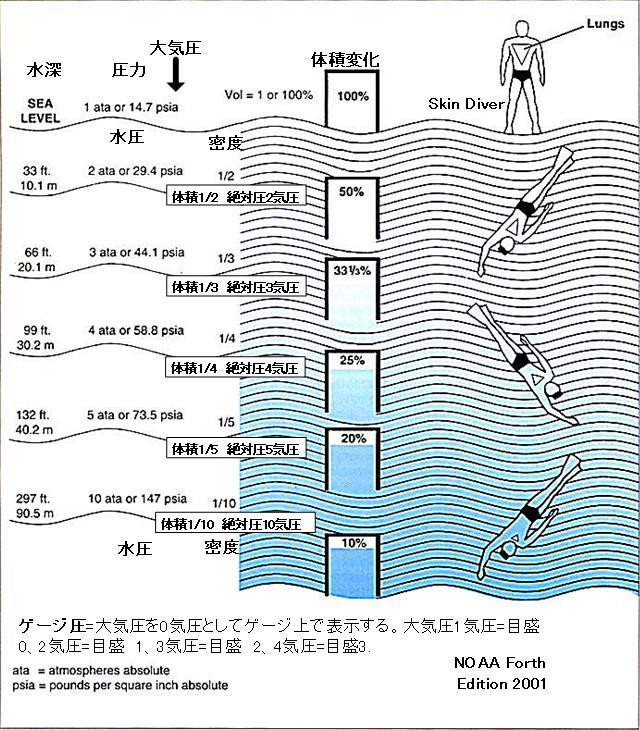
��C��(��C�̏d��)�A�Ð����A�Q�[�W���A��Έ�.
�n��0m�A���͊C�ʂŎ鈳�͂��C���ƌ����A�C�ʉ��Ŏ鈳�͂�Ð����ƌ����B
�^����[���Ƃ�����Έ����ɑ��āA�Q�[�W���͑�C�����[���Ƃ���A���ΓI�Ȉ��́B
1ata(��Έ���)�@1atm(��C��)�@1atg(�Q�[�W��)�@�������̓Q�[�W�������[(m)/10
��Έ���(ata)���Q�[�W����(atg)+��C��(atm)�����[(m)/10+1
��Έ� = �Q�[�W�� + ��C��
�Q�[�W�� = ��Έ� - ��C��
�Q�[�W���\��
�Q�[�W���͋@�B�I�Ɏ��o�Ō���ׂɁA��C����0�s/㎠�Ƃ��A1�s/㎠����\������B
�܂�A��C��1�s/㎠��0�_�Ƃ��āA2�s/㎠��ڐ�1�A3�s/㎠��ڐ�2�ƕ\������B

��C���Ƃ́A��C(��C)�ɉ����Đg�̂��ׂĂɍ�p���āA��C(��C)�K�X�̏d���ɂ���Đ�����ׁA��C���͓���ȓ_�ł͖����A����������Ɍ����č�p����B
�܂�A��C���͂���������ɉ����ē������̂ŁA���̉e���͑��E�����B
�C�ʂł̑�C��(��C�̏d��)��14.7psi�A����1.03�s/㎠�ɓ������B�������A���x�������A���̒l�͌�������B
14.7psi(1.03�s/㎠)�ȏ�̈��͎͂��Ƃ��ċC���ŕ\����邪�A1�C����14.7psi�ɓ������A10�C����147psi�A100�C����1470psi�ɓ������B
��C���ɉ����āA�C�ʏ�ł̋C����1013.25hPa�� ����A�ፂ�x�ł�10m�̏㏸�ɑ���1hPa���C�����ቺ���Ă����B����́A�R�֓o�����肷 �鎞�A���̖ڈ��Ƃ��Ȃ�B
���̑�C���̋�C���C�ʏ�ƒW���ʏ�ɋ�C�̒��Ƃ��ė��Ă��ꍇ�A�C�ʏ�ł̈��ٍ͈͂����Ă��܂����A����͊C���ƒW���ł̖��x�̈Ⴂ�ɂ���Đ�������̂ł���B
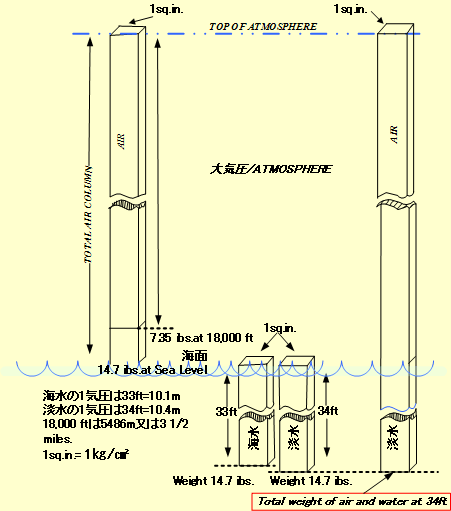
���̊C����ƒW����ŋN���鈳�͍��́A���Ƃ��ĎR�̏�̌�_�����Ő��鎞�ɖ��ƂȂ�ׁA�C���̐��[�ݒ�\������B�܂��A�����W���ł̒ʏ�����ƌ��������ł������_��A���S��~�_���Ⴄ�ׂɒ��ӂ��K�v�ł���B
�C���ł�1�C��=14.7ibs=1Kg/㎠�@2�C���ł͐��[10.1m��10m�ƂȂ�B
�W���ł�1�C��=14.7ibs=1Kg/㎠�@2�C���ł͐��[10.4m�ƂȂ��Ė����o���Ȃ��B
ibs=psi
�Ð����Ƃ́A��(���͉t��)�̏d���ɂ���Đ����A����(���͉t��)�̐g�̂��ׂĂɍ�p���邪�A��C���̗l�ɐÐ����́A����̐[�x�ł͂���������ɉ����ē�������p����B
�_�C�o�[�ɂƂ��čł��d�v�Ȉ��͂Ƃ͐Ð����̎��ł���B
�Ð����ł̊C��������~����ꍇ�A1�t�B�[�g������0.445psi(1Kg/㎠/9.75m)�̊����ő������A�W��������~����ꍇ�́A1�t�B�[�g������0.432psi(1Kg/㎠/10m)�̊����ő�������B
�Q�[�W���Ƃ́A��Έ��͂Ɠ���̈��͂̍��ł���A���͂͋�C�ɐڂ��Ă���C�ʂŃ[���ƂȂ�Q�[�W�ő��肳���B
���ׂ̈ɃQ�[�W���́A�ڐ��肪psi�̎��ɂ�14.7�������鎖�ɂ���āA�܂��͖ڐ��肪1Kg/㎠�̎��ɂ�1.03�������鎖�ɂ���Đ�Έ��͂ɕς�����B
��Έ����Ƃ͑�C���Ɛ����̕��̂ɂ�����Ð����̍��v�B
��Έ��͂̕\���̓|���h/�����C���`(psia)�A�܂��́A1Kg/㎠�ŕ\�킳���Bpound/square inch(psi)
���x�Ƃ͒P�ʑ̐ϓ�����̎���(1cm3)�@�C�̂̏ꍇ��ℓ���g���B
���x�̌�����
�@�@�@�@�@�@�@�@�@�@�@�@�@�����̎���(g)
�����̎���(g)
�@ ���x(g/cm3)=�@�@�@�@�@�@�@�@�@�@�@�@�@�@
�����̑̐�(cm3)=
�����̑̐�(cm3)
���x(g/cm3)
�����̎���(g)=���x(g/cm3)�~�����̑̐�(cm3)
���̖��x(1g/cm3)��肻�̕��̖̂��x���傫�����́A���̕����͐��ɒ��݁A���̖��x(1g/cm3)��肻�̕��̖̂��x�����������́A���̕����͐��ɕ����B
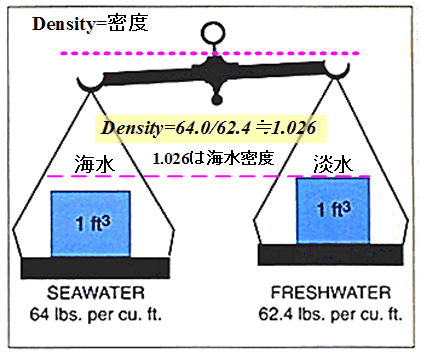
�ł́A�������̗l�ȏ�Ԃ�����Ă��邩�ƌ����ƁA���x�̊W������A���͊���x1�Ƃ� ��ƁA�C���̖��x�ł�1.025(�C������x)�ƂȂ�A�e��1���b�g���̒��ɒW���ƊC������� �Ĕ�r����ƁA�C���̕���25�f�V���b�g�������d�������ƂȂ�B��
���x�Ŕ�r���Č���Ɓ@(�P��: g/cm3 = 103kg/m3)
1.0 kg/m3 = 1000 g/1000000 cm3 = 0.001 g/cm3
= 0.001 kg/L
���� �@ = 19.3g/cm3
���E���� = 18.7
���� = 11.3
���� = 8.92
���S = 7.874
���A���~�j�E�� = 2.70
���}�O�l�V�E�� = 1.75
���� = 1.00g/cm3
���C�� = 1.025g/cm3
����C = 0.0012g/cm3
���X = 0.917g/cm3
���K���X = 2.4g/cm3
���C���ƒW��������(�d��)�Ƃ��Č���ƁA�̐ςƂ��ĊC���̕������Ȃ��Ȃ�B
�܂�A�C���̕����d�����B�̐ς��Ƃ��Č���ƁA�C���̕����d�����B
��d�Ƃ��Č����ꍇ�A�W��1�͊C��0.97���d�����B���̎��͕��͂Ƃ��Ă����Ď���B
�_�C�o�[���W�����ƕ����炢���A�C�����Ɨǂ������B
��d�Ɩ��x�̒l�́ACGS�P�ʌn�ŕ\���ƁC���l�I�ɂقړ����l
�E�G�C�g�R���g���[���K�g�����ĎQ�l�ɂ��ĉ������B
----------------------------------�w�E�B�L�y�f�B�A�iWikipedia�j�x----------------
2a.��d�i�Ђ��イ�Aspecific
gravity�j�Ƃ́A
���������̎����ƁA��������̐ς̊�ƂȂ镨���̎��ʂƂ̔��ł���B
�ʏ�A�ő̋y�щt�̂ɂ��Ă͐��i���x���w�肵�Ȃ��ꍇ��4���j�A�C�̂ɂ��ẮA�����x�A�����͂ł̋�C����Ƃ���B
���ʓ��m�̔�ł���̂Ŗ������ʂƂȂ�B�ʏ�̐��i�������j�̖�4���ł̑�C�����̋�C�����n���Ă��Ȃ��Ƃ��̖��x��0.999972g/cm3�ŁA�قƂ��1.0g/cm3�ł��邩��A��d�Ɩ��x�̒l�́ACGS�P�ʌn�ŕ\���ƁC���l�I�ɂقړ����l�ƂȂ�B
�܂��A��d��1�����傫�������͐��ɒ��݁A1���������������͐��ɕ����B
���x�Ɣ�d�͍�������₷�����A���x�͎��ʂ�̐ςŊ������ʂł���A��d�͊�����Ɣ�ׂ����ʔ�ł���Ƃ����_�ňقȂ������̂ł���B
����āA���������ɕ������ނƂ����̂́A���x������d�ɂ���Ă̕������f���₷���B
�@�@�@�@�@�@�@�@-�t���[�S�Ȏ��T�w�E�B�L�y�f�B�A�iWikipedia�j�x�̔�d�̍������p���Ă��܂��B-
�����̕��̂́A���̕��̂������̂������̏d�ʂ����y���Ȃ�A
F= -��V g
F:����[N]�A��:���̖��x[kg/m3]�AV:���̂̐��v���Ă��镔���̑̐�[m3]�Ag:�d�͉����x[m/s2]
�Ȃ����̖@���͐������łȂ��S�Ă̗��̂ɂ��ē��Ă͂܂�B���͂̑傫���͗��̒��ɂ��镨�̖̂��x�ɂ͊W���Ȃ����A���̂������̖̂��x���������ꍇ�ɂ͏d�͂ƕ��͂͒ނ肠���B
���Ȃ킿
��Vg=mg�@�@m:���̂̎���[kg]
m=��V�ł��邽�߁A���̖̂��x�������m�ł����V�𑪒肷�邱�Ƃŕ��̂̎��ʂ𐳊m�ɒm�邱�Ƃ��ł���B
���ɕX�������Ă��Ă��̕X�������Ă����ꍇ�A�������X�̎��ʂ���m �Ƃ���Ɛ��̑̐ς���m/�� �����������邪�A��̎�������m=�χ�V�A��V=��m/���ł��邽�ߕX�̐��v���Ă��镔���̑̐ς���m/�� ������������B
����āA���̑̐ϑ������ƕX�̐��v�̐ό��������������Ȃ�A�X�������Ă����ʂ͕ω����Ȃ����ƂɂȂ�B
�E�G�C�g�R���g���[���K�g���������͂Ƃ� ���Q�Ƃ��ĉ������B
���͉��x���������čs���ƁA�d�����Ȃ艺���ւƒ���ōs�����A���x��4���ȉ��ɂȂ�ƁA���x�͋t�Ɍy���Ȃ�̂ł���B
�Ⴆ�A���x��0���ȉ��ƂȂ��Đ�������Ƃ��̕��͂ɂ���ĕ������ƂȂ�B
���̕X��X�R�����̗�ɓ��Ă͂܂�A���ʂ��瓀��n�߂�B
�܂��A�C�m�[�w���ɂ����Ă͂܂邪�A������̏ꍇ�͐[�w�ɒ��ݐꂸ�ɕ\�ʂɕ����A���ʂœ��������̂��X�ł���A����Ă�����̂����X���B
�ł́A�[�w���̏ꍇ�͂������ƒ���ł�������₳�ꂽ�C���́A�r����4���ȉ��ƂȂ邪�A�����ɂ��C�����x�������ׂɁA���̂܂܊C��[������ōs���B
�X�ɁA�������Ⴂ�Ɛ��̔S�����オ�鎖�őD�������x���Ȃ鎖������Ă���A���R�Ƃ��āA�����������Ɛ��̔S�����Ⴂ�ׂɑD���������B
1����32���ł̏ꍇ�A���������S����2�{�ƂȂ�B�@�S��=Viscosity
3.�_���g���̖@��(�����̖@��)�@�sDalton's Law�t
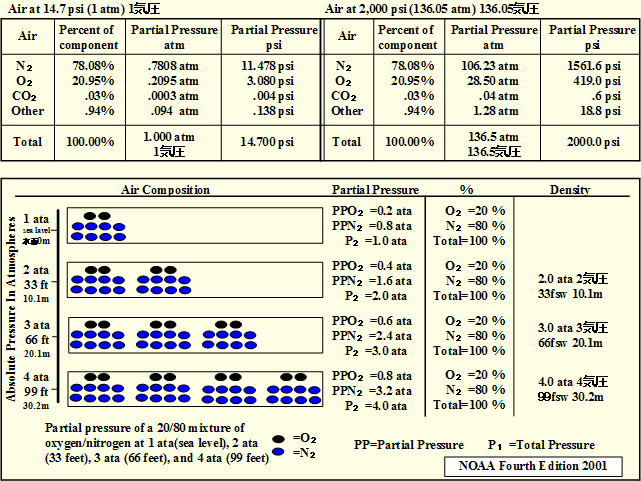
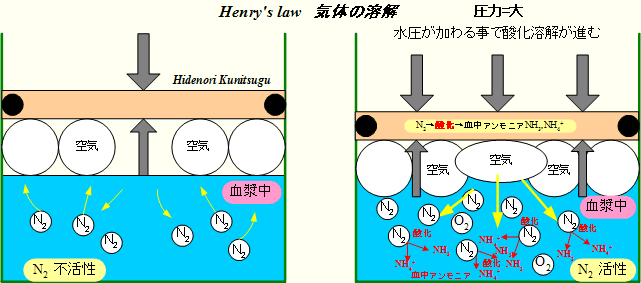
4.�w�����[�̖@��(���͉��ɉ�����C�̗̂n��)�@Henry's Law
"���鉷�x�̉t�̂ɗn������C�̗̂ʂ́A�t�̂ɐڐG���Ă���C�̂̕����A�y�щt�̂ւ̋C�̗̂n���ɂ���Č��肷��"
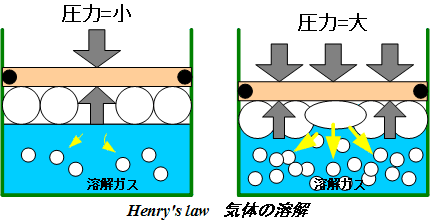
���̗�̓X�L���[�o�_�C�o�[�̔x��\���Ă��āA���傤�ǐ��ʂ͔x�E�̌������ɓ�����A���t�ʂ͌����B
���[10m��2�C���A���[20m��3�C���ƂȂ�A���͂������Ȃ�ɂ�Ē��fN2�������ɗn�����ޗʂ������Ȃ�B�_�fO2�A��_���Y�fCO2��������ɗn����B
���̓��ւƎ�荞�܂ꂽ��C����(�_�fO2�A���fN2�A��_���Y�fCO2)�͔x�זE���ɉ����ĕK�v�ȕ�������荞�܂�܂��B
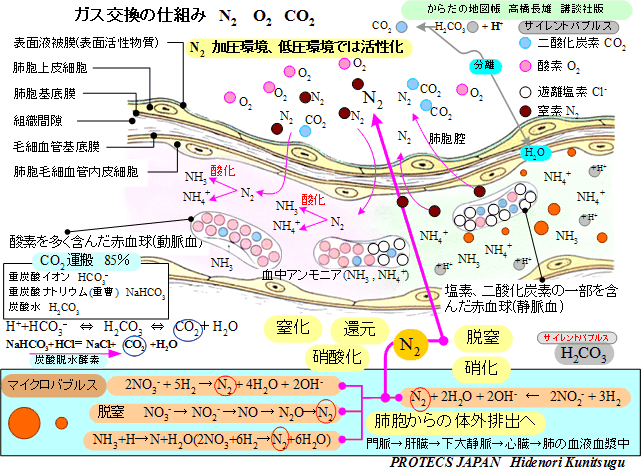
�v�`�F�b�N
�n�������Ƃ��钂�fN2�͔x�Ŗ\�I����āA�O�����Ƒ̓����̍��̕�(���t����܂�)�̒��fN2����荞�����Ƃ��邪�A�x�ł̓������э��Ǔ��̌��t�̌������ɉ����Ď_������ăA�����j�ANH3�A�A�����j�E���C�I��NH4+�A�A�_C5N4N4O3�A�A�fNH2CONH2���ɕ�����������đ̓��ւƐZ�����čs���܂��B���ɐ��n���Ŏ��n���̃A�����j�ANH3�͑̉t1ml�ӂ�442ml(442�{)���n����̂ł��������h���L������A�Ő���тт܂��B
�������A�A�����j�ANH3�͑̓��ɉ����đ唼�̕����L���Ŗ��łȃA�����j�E���C�I��NH4+�Ƃ��đ��݂��A���̂̍P�퐫�@�\�ɉ�݂��Ă���̂ł��B
���̃w�����[�̖@���́A�����ɂ���������a(������)�ƌ����錸���ǂ̌��ɂȂ��Ă��܂��B
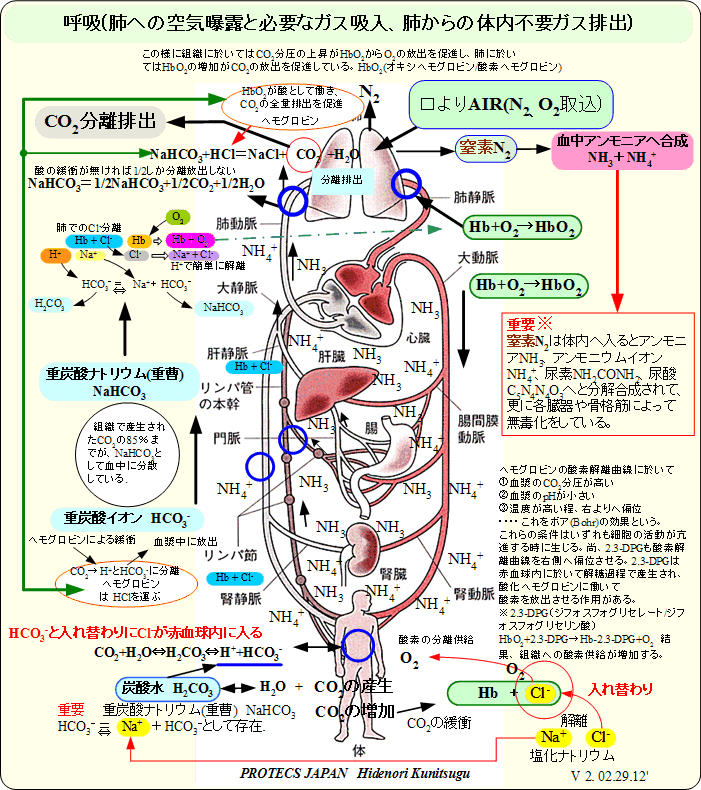
�ċz�ɂ���Ĕx����z�����ꂽ���f�͌��t����đS�g�̑g�D�ւƉ^��A�g�D�̒`�����̐����ƌ��ѕt���Ղ��̂ł��B
�z�����ꂽ���f�́A�O���̈��͂̒ጸ�ɂ���Ĕr�o���悤�Ɠ����܂����A�r�o�̏ꍇ�́A�z�������r�o�Ɏ��Ԃ��|����̂ł��B
����́A�e�g�D����̒��f�̐藣���I���w�ω����N���邩��Ȃ̂ł��B
�ڂ����͌����ǂ̍����Q�Ƃ��ĉ������B
�n��ɉ�����l�̂ɂ́A����1�C�����̋�C�K�X(�_���g���̕����̖@���Q��)���Z���z������āA�̓��Ƒ̊O�̈��͋ύt������Ă��܂��B
�����I�ȗ͂ɂ���đ̓��Ɏ�荞�܂�A���w�I�ω��̎�e�ɂ���đ̓��̊e�g�D�ɋz������čs���܂��B
���fN2�̉��w�I�ω� �_�����ɉ��������E�Ҍ��@�@�_�����ɉ����_���������E�Ҍ��E�E��.
�܂�A���f�͑̓��ł�N2�P�̂Ƃ��āA�ق�̋͂��������݂��Ȃ��̂ł��B
�w�����[�̖@���ɂ��t�̒�(����)�ւ̋�C�K�X�̋z���͒��fN2�A�_�fO2�A��_���Y�fCO2�����n�����݁A�S�g�ւƉ^��邪�A���fN2���唼�ŁA�_�fO2���_���Y�fCO2���͑����͖����B
����́A�_�fO2���_���Y�fCO2�̓w���O���r��(�Ԍ���)�ɂĉ^���Ɣr�o���s���Ă��邩��ƌ����Ă����B
�Q�l�@�ċz�@�ɂ����@���t�̏z���@���t�Ƃ͉�?�@�������@
Henry's law stated
mathematically
VG�@�@
=�� P₁�@
VL
VG=Volume of gas dissolved at STPD STPD(�W�����x�ƈ���)�ŗn�������C�̗̂e��.
(standard temperature pressure dry).
VL=Volume of the liquid.
�t�̗̂e��.
��
=Solubility
coefficient at specified temperatures. ���艷�x�ł̃u���\���n��x�W��.
P₁=Partial pressure
of that gas above the liquid. �t�̏�̋C�̂̕���.
�_���g���̖@���A�w�����[�̖@���̓X�L���[�o�_�C�r���O�ɉ����āA�����a�������ǂɌW��ׁA�L���ɗ��߁A�o���ĖႢ�����B
5.�ċz�K�X�̎��x�A���I�A�����蓙.
6.���̋��܁E�U���E�z���Ǝ��o�A���̌����ƌ��F.
7.�����̉�.
�y�u�X�L���[�o�_�C�o�[�v�����̐g�����ׂ̗\���m���z study-four_b����study-four_c��